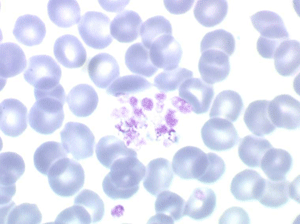
Pathologie des plaquettes
1 – Physiologie des plaquettes
Les plaquettes naissent dans la moelle osseuse par fragmentation du cytoplasme des mégacaryocytes. Le mégacaryocyte est une cellule géante qui croît par endomitose (division du noyau sans division du cytoplasme) et dont le nombre absolu dans la moelle est donc très faible. Les fragments cytoplasmiques, ou plaquettes, passent dans la circulation sanguine et y exercent leur fonction hémostatique. Leur durée de vie dans le sang est d'environ 8 jours. Sur lame de sang elles apparaissent comme des petits éléments granuleux, dépourvus de noyau, de couleur pourpre, grossièrement arrondis, irréguliers, de 2 à 5µ de diamètre. On peut y distinguer 2 parties, une partie périphérique hyaline (hyalomère) et une partie centrale granuleuse (chromomère), les grains y sont de plusieurs types (granules alpha, granules denses, etc.) et contiennent divers facteurs intervenant dans l'hémostase (facteur 4, facteur Von Willebrand, etc.). Sur lame, les plaquettes sont soit isolées, soit groupées en petits amas car elles ont une forte tendance à l'agrégation.
Le taux normal de plaquettes sanguines se situe entre 120.000 et 450.000/µl.
La fonction biologique des plaquettes est hémostatique. Elles forment le clou plaquettaire qui obture les brèches se produisant sur les parois vasculaires (hémostase primaire). Les plaquettes n'agissent pas seules, elles interagissent avec des facteurs vasculaires (endothélium, vasoconstriction, hémodynamique), avec les autres cellules sanguines (notamment les globules rouges) et avec les facteurs enzymatiques de la coagulation (prothrombine, fibrinogène) et de la fibrinolyse. En cas de brèche vasculaire les plaquettes adhèrent à l'endothélium lésé (rôle important du facteur Von Willebrand endothélial et plaquettaire) et sécrètent des facteurs (ADP, Thromboxanes, PAF, etc.) favorisant leur recrutement et leurs liens entre elles, c'est à dire leur agrégation en un thrombus. Lors de la formation de ce thrombus les plaquettes libèrent des enzymes activant la coagulation, notamment la transformation de la prothrombine en thrombine, elles sont ensuite impliquées dans la rétraction du caillot.
Les plaquettes jouent aussi un rôle dans l'imperméabilité vasculaire. En cas de thrombopénie les microvaisseaux deviennent perméables, les globules rouges traversent plus facilement la paroi vasculaire et cette extravasation sanguine est responsable du phénomène clinique du purpura. Les plaquettes non consommées par le clou plaquettaire sont détruites par les macrophages de la rate et du foie.
Une méthode simple pour tester la valeur fonctionnelle des plaquettes est le « temps de saignement ».
2 – Pathologie des plaquettes
La pathologie plaquettaire comporte 3 chapitres : les thrombopénies, les thrombocytoses et les thrombopathies.
Thrombopénies
La thrombopénie se définit par un taux de plaquettes inférieur à 120.000/µl. Cette diminution du nombre de plaquettes circulantes entraine un risque hémorragique. Cependant ce risque dépend de 2 facteurs : le nombre de plaquettes et la rapidité d'apparition de la thrombopénie. En fonction du nombre de plaquettes le risque est :
• très faible entre 50.000 et 100.000/µl,
• aléatoire entre 20.000 et 50.000/µl,
• important en dessous de 20.000/µl.
Mais le risque est nettement accru si la thrombopénie est aiguë.
Il existe de fausses thrombopénies, dues à l'agglutination des plaquettes par l'anticoagulant utilisé pour le prélèvement. Les amas de plaquettes qui se forment alors sont comptabilisés comme globules blancs par l'automate et les quelques plaquettes isolées comptées comme telles donnent un nombre abaissé. Devant toute thrombopénie il faut donc vérifier l'absence de plaquettes sur la lame colorée et en cas de doute refaire un prélèvement en Unopet. Les thrombopénies peuvent être d'origine centrale (insuffisance de production médullaire) ou périphérique (excès de destruction par la rate et le foie ou consommation).
1 – Les thrombopénies centrales sont rarement isolées, elles s'accompagnent habituellement des autres stigmates d'une insuffisance médullaire : une anémie non régénérative et une neutropénie. La moelle est pauvre en mégacaryocytes. Les étiologies sont les mêmes que celles de toute insuffisance médullaire, soit une aplasie de la moelle (insuffisance quantitative), soit une myélodysplasie (insuffisance qualitative). Dans ce dernier cas une thrombopénie isolée, chronique et progressive, peut être le signe initial, mais c'est beaucoup plus rare que le début par une anémie (anémie réfractaire).
2 – Les thrombopénies périphériques sont dues à une destruction des plaquettes, le plus fréquemment par des auto-anticorps (maladie auto-immune). La thrombopénie est isolée (absence d'anémie et de neutropénie), le sang est pauvre en plaquettes mais la moelle est riche en mégacaryocytes. Ces thrombopénies sont souvent graves car très hémorragiques du fait de leur rapidité d'apparition, en quelques heures ou jours. Les étiologies en sont variées mais dominées par une maladie : le Purpura Thrombopénique Idiopathique.
(1) Le Purpura Thrombopénique Idiopathique (PTI) atteint des sujets jeunes, est d'apparition brutale, parfois déclenché par une infection virale, se traduit par des hémorragies cutanées (purpura) et entraine une disparition quasi totale des plaquettes sur la lame de sang. Le PTI est une urgence hématologique et demande un traitement rapide. Passée la phase aiguë particulièrement grave par le risque d'hémorragies viscérales (notamment cérébrales) l'évolution est variable : guérison, rechutes (notamment lors d'infections) ou chronicité.
(2) Les autres causes de thrombopénies périphériques sont :
• des infections virales : maladies éruptives, mononucléose infectieuse, virus HIV,
• une toxicité médicamenteuse : héparine, sulfamides.
• une CIVD (coagulopathie de consommation), notamment dans la maladie de Moschowitz ou Purpura Thrombotique Thrombopénique (PTT), autre urgence hématologique où la thrombopénie s'accompagne d'une anémie régénérative avec schizocytose sanguine (cf. « Sangs pathologiques » → « Globules rouges » → « Cytologie des anémies »),
• l'hypersplénisme (splénomégalies d'origines diverses) qui rappelle que la rate est le principal organe du système macrophage destructeur de plaquettes,
• les thrombopénies néonatales par des anticorps anti plaquettes maternels.
Thrombocytoses
Les thrombocytoses se définissent par une augmentation du taux de plaquettes au dessus de 500.000/µl. Au dessus de 1 million on parle de thrombocytémie. Cette augmentation des plaquettes entraine un double risque de thromboses et d'hémorragies, ces dernières étant dues à une altération de l'activité biologique des plaquettes proportionnelle à leur taux, c'est dire que ce risque est surtout réel dans les thrombocytémies.
L'examen sur lame des plaquettes peut montrer soit de nombreuses plaquettes isolées, bien détachées les unes des autres, soit des amas de plaquettes agrégées, parfois très grands, et le chiffre des plaquettes fourni par l'automate peut alors être sous-estimé. Devant un chiffre anormal de plaquettes l'examen cytologique de la lame de sang colorée doit donc être la règle.
Les thrombocytoses peuvent être secondaires ou primitives.
1 – Les thrombocytoses secondaires se situent habituellement entre 500.000 et 800.000/µl. Elles sont parfaitement tolérées et ne donnent lieu à aucune complication.
• L'étiologie la plus fréquente est la régénération médullaire après une hémorragie, une hémolyse ou une sortie d'aplasie. L'augmentation des plaquettes s'associe alors à une anémie régénérative et une polynucléose et est transitoire.
• Une cause particulière de thrombocytose persistante est la splénectomie. L'ablation de la rate (après un traumatisme par exemple) enlève une grande partie du système macrophage, ce qui explique aisément cette thrombocytose par défaut de destruction. L'examen de la lame de sang montrera aussi la présence de nombreux corps de Jolly intra-érythrocytaires, pour la même raison de non épuration des restes nucléaires des globules rouges par le système macrophage.
• On peut observer une thrombocytose modérée au cours de syndromes inflammatoires associés à des cancers ou des lymphomes (maladie de Hodgkin notamment).
2 – La thrombocytose primitive, ou thrombocytémie essentielle, a été traitée et illustrée dans le chapitre des « syndromes myéloprolifératifs » dont elle fait partie intégrante (cf. « Sangs pathologiques » → « Lignée granuleuse » → « Myélémies et syndromes myéloprolifératifs »). On peut observer une thrombocytose importante dans certaines myélodysplasies primitives : anémie sidéroblastique (ASIA) et syndrome 5q-, qui ont été traitées et illustrées dans le chapitre correspondant (cf. « Sangs pathologiques » → « Lignée granuleuse » → « Myélodysplasies»).
Rappelons ici qu'il existe une leucémie à mégacaryocytes (LAM7 de la classification FAB) avec passage dans le sang de micromégacaryoblastes ayant la morphologie de lymphoblastes à expansions périphériques (blastes à « oreilles). L'insuffisance médullaire, liée à la leucémie ainsi qu'à une fréquente myélofibrose, entraine une thrombopénie.
Thrombopathies
Les thrombopathies se définissent comme des plaquettes en nombre normal mais ayant une activité biologique déficiente. L'aspect des plaquettes est habituellement normal sur lame. Les thrombopathies peuvent être acquises ou congénitales.
• Les thrombopathies acquises sont dues soit à des médicaments (aspirine, antiagrégants plaquettaires), soit à une macroglobulinémie (maladie de Waldenstrom), la macroglobuline est directement responsable de la thrombopathie par un enrobement des plaquettes qui inhibe leur agrégation.
• Les thrombopathies congénitales sont rares, nous ne ferons que citer la thrombasthénie de Glanzmann (absence d'agrégation des plaquettes) et la dystrophie thrombocytaire de Bernard et Soulier (défaut d'adhésivité des plaquettes à l'endothélium vasculaire) qui peut comporter des plaquettes géantes.